バイオ医薬品製造のスケールアップにおける真のボトルネックは、製造能力ではなく需要予測にある
キーポイント
バイオ医薬品のスケールアップにおける最大の障壁は、製造キャパシティではなく「需要の不確実性」
多くの開発プログラムは、ステンレス設備への投資を正当化できる生産量に達しない
5,000Lクラスのシングルユースシステムは、需要が読みづらい環境下で高い柔軟性を発揮
需要主導型の柔軟なアプローチにより、より賢明な設備投資と迅速な市場対応が可能になる
バイオ医薬品のスケールアップが難しい理由は、製造キャパシティが不足しているからではありません。
本当の課題は、「需要が予測できないこと」にあります。
開発プログラムが後期段階に近づく頃、開発チームは市場の見通しが十分に立たないまま、将来の生産量を見据えた極めて重要な意思決定を迫られます。需要予測は変動し、臨床試験の登録状況は揺れ動き、競合環境も刻々と変化します。それでもなお、数年先のプログラムの行方を左右しかねない製造戦略を、この段階で確定させることが求められるのです。
多くのバイオテック企業や製薬企業は、スケールアップにおける最大のリスクは「十分なキャパシティを確保できるかどうか」だと考えがちです。しかし、真の課題はより早い段階に存在し、さらに本質的です。それは、過剰投資にも不足投資にも陥らないよう、需要曲線をどこまで正確に見極められるかという点にあります。
そしてまさにこの課題に対して有効なのが、5,000Lクラスのシングルユースバイオリアクター(S.U.B.)を基盤とした柔軟な製造プラットフォームです。このアプローチにより、リスクを低減し、制約を取り払い、市場の不確実性が残る段階であっても、CDMOパートナーとともに自信を持って次のステップへ進むことが可能になります。
「完全な確実性」を待つ必要はありません。
スケールアップの壁は、キャパシティではない
製造キャパシティは制約のように感じられがちですが、実際には、多くのバイオ医薬品が大規模なステンレス設備を必要とする生産量に到達することはありません。
近年の業界分析によると、後期開発段階にある分子の大半は、2,000~5,000L規模の生産量に収まっていることが示されています(2023年 CPHI Annual Report)。
つまり、巨額の固定資産投資を正当化できるプログラムはごく一部に限られるのです。
この現実は、従来の「将来を見越して大規模設備を確保する」という発想を見直す必要性を示しています。スケールアップにおける真の課題は、キャパシティ不足ではなく、需要の不確実性に柔軟に対応できないことにあるのです。
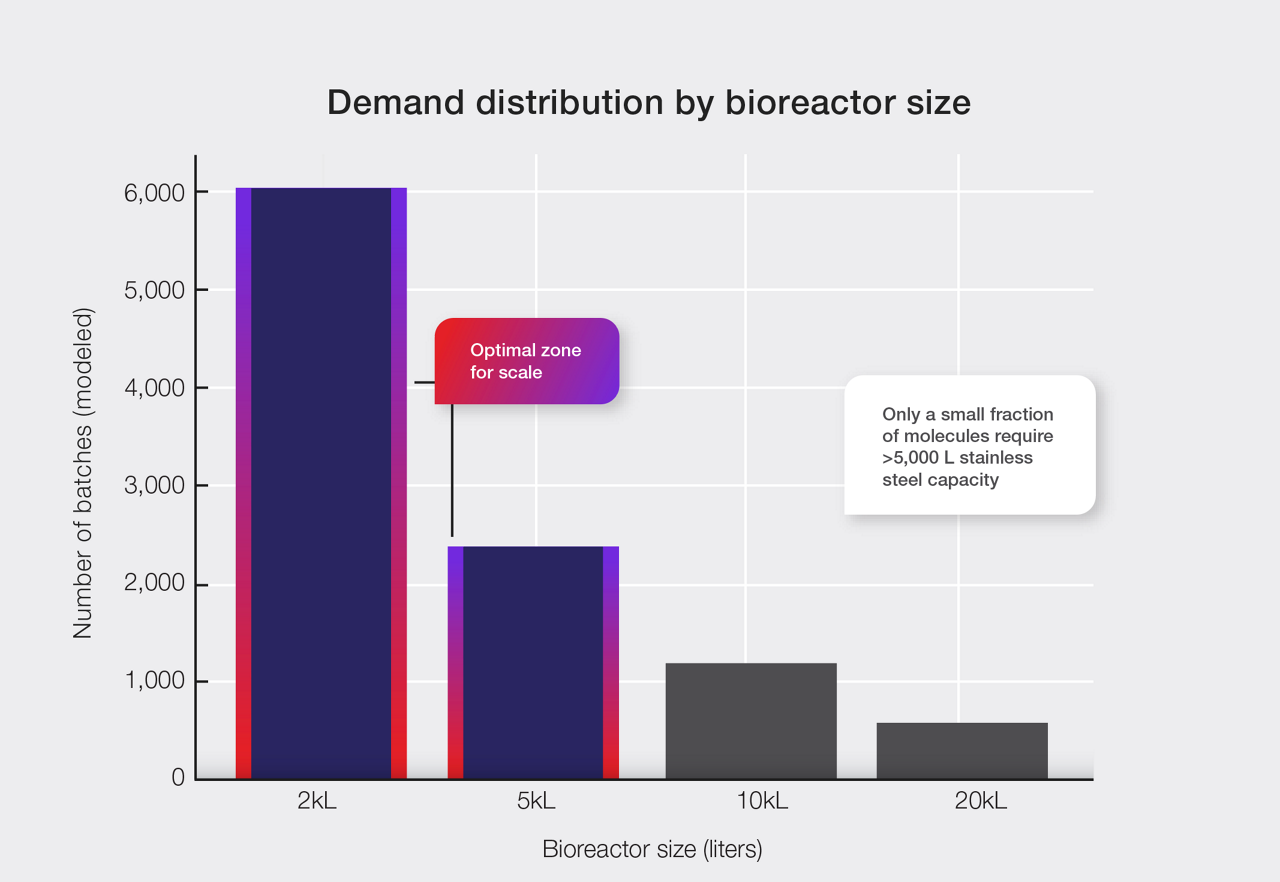
現在のバイオ医薬品パイプラインにおける需要データを俯瞰すると、ある明確な傾向が浮かび上がります。
後期段階に進んだ多くのバイオ医薬品でも、巨大なバイオ製造設備が必要になるケースは限られています。
この現実が、スケールアップ戦略における慢性的なジレンマを生み出しています。
将来需要を過大に見積もれば、使われない可能性のある設備に対して、巨額の設備投資や運用コストを固定化してしまいます。
将来需要を過小に見積もれば、需要が急拡大した際に供給が追いつかず、成長機会を逃すリスクが高まります。
多くの開発プログラムが位置するのは、この「中間ゾーン」です。
そこを支配しているのは不確実性であり、その不確実性こそが、あらゆるスケール判断を“賭け”にしてしまいます。
つまり、**大半のプログラムにおいて価値を生むのは「生産量」ではなく「柔軟性」**なのです。
実現するか分からない将来の大量生産を前提に計画を立てるのではなく、実際の需要に応じてリアルタイムに適応できるスケーラブルなモデルを採用することが、より合理的な選択となります。
後期開発段階のチームが本当に必要としているのは、単なるキャパシティの増強ではありません。
自分たちの歩みに合わせて柔軟に変化できるキャパシティです。
**5,000Lクラスのシングルユースバイオリアクター(S.U.B.)**を活用すれば、キャパシティはもはやボトルネックではなくなります。需要が顕在化すれば迅速にスケールアップでき、予測が変わればスケールダウンも可能です。しかも、長期にわたる検証や固定的な設備投資に縛られる必要はありません。
この柔軟性により、CDMOはスポンサーの需要の変化に合わせて生産能力を調整できます。
スポンサーが、あらかじめ決められたキャパシティに自らを合わせる必要はありません。
CDMOの役割:スポンサーが不確実性に悩まなくて済む環境をつくること
後期開発段階にあるスポンサーにとって、理想的な製造パートナーとは、需要の変動に柔軟に対応でき、時期尚早な意思決定を強いないCDMOです。
5,000Lクラスのシングルユース技術(S.U.T.)プラットフォームを基盤とするCDMOは、次のような価値を提供します。
キャパシティを迅速に増減できる
ステンレス設備に伴う硬直的で長期的な立ち上げスケジュールを回避できる
臨床バッチから商業バッチへの移行をスムーズに支援できる
需要予測が変化しても、プログラムの遅延リスクを抑えられる
固定的な設備に生産計画を縛るのではなく、スポンサーの実際の需要に合わせてキャパシティを調整する。
需要が顕在化すれば拡張し、そうでなければ抑制する――この柔軟な運用が可能になります。
この動的な製造モデルは、開発企業が直面する本当のリスクに正面から応えます。
それは、キャパシティ不足ではなく、「キャパシティを早期に確定してしまうこと」そのものなのです。
5,000Lシングルユースシステムが変えるバイオ医薬品スケールアップの考え方
5,000Lクラスのシングルユース技術(S.U.T.)、特に HyPerforma™ DynaDrive™ シングルユースバイオリアクターは、スポンサーに長期の立ち上げ期間、回収困難な設備投資、運用の硬直性を強いることなく、スケールアップを可能にします。
真の柔軟性:需要の変化に応じて、自在にスケールアップ/ダウン
DynaDrive 5,000L シングルユース技術(S.U.T.)は、幅広いプロセス移管と予測可能なスケールアップを可能にし、開発チームに次の価値を提供します。
初期開発から後期開発まで、スムーズに製造を移行
ダウンタイムや制約を最小限に抑えながら、キャパシティを柔軟に調整
臨床試験の被験者登録状況、市場動向、競争環境の変化にも迅速に対応
さらに、5,000Lシステムを2基以上組み合わせて運用(マルチプレックス)することで、高い生産量を実現しながらも、俊敏性を損なうことはありません。

小~中規模プログラムには 5,000L S.U.B. ×1基、
大規模プログラムには 5,000L S.U.B. ×2基
コスト効率の向上:過剰投資を回避し、リスクを最小化
シングルユース技術(S.U.T.)**は、ステンレス設備に伴う巨額の設備投資を不要にすると同時に、洗浄・滅菌・バリデーションといった工程負荷を削減し、開発スピードを妨げる要因を取り除きます。
開発企業にとって、これは次のメリットを意味します。
初期投資リスクの低減
キャパシティ立ち上げの迅速化
運用コストの削減
需要に応じて生産規模を継続的に最適化できる柔軟性
その結果、スポンサーは需要が明確になったタイミングで投資を行うことが可能となり、数年先を見越して先行投資を行う必要がなくなります。
サステナビリティ:現代の期待に応える設計
5,000Lシングルユースバイオリアクター(S.U.B.)は、運用面でのメリットにとどまらず、次のような点で環境負荷の低減にも貢献します。
水使用量の削減
エネルギー消費量の低減
施設フットプリントの縮小
CIP/SIPに必要なユーティリティの削減
これにより、1バッチあたりの生産性を高めながら、全体としての資源投入量を抑制することが可能になります。
多くのバイオテック企業がパートナー選定において重視するサステナビリティの観点にも、しっかりと合致したアプローチです
成長戦略を、もっと柔軟に。
バイオ医薬品開発の新しい選択肢
不確実性は、バイオ医薬品開発において常につきものです。
しかし、適切な製造戦略とCDMOパートナーを選べば、キャパシティや需要の不確実性が、開発の成否を左右する要因である必要はありません。
柔軟で需要主導型の製造モデルは、スポンサーに次の力をもたらします。
需要予測が変化しても、自信を持って意思決定できる
財務面・運用面のリスクを抑制できる
後期開発段階においても、プログラムを滞りなく前進させられる
機会が訪れた瞬間に対応しつつ、過度な先行投資を避けられる
Thermo Fisher Scientificのバイオ医薬品向けCDMOサービスでは、50Lから5,000Lまでのシングルユースバイオリアクター(S.U.B.)を活用し、需要に応じた柔軟な製造を可能にしています。
その結果、スケールアップは大きな先行投資を伴うリスクの高い判断ではなく、状況に応じて調整できる、計画的で俊敏なプロセスへと変わります。
すべてのスポンサーにとって、より確かな成長への道筋を。


