ブログ - Solved With Heart & Science
技術・科学分野の専門家による記事
最新の科学イノベーションや医薬品開発の大きな進歩、業界の動向を深く掘り下げるインサイトなどを提供するブログです。カテゴリー別にブログを検索してください。検索結果はサムネール表示またはリスト表示することができます。
ご興味ある内容はどちらですか?

ブログ
バイオ医薬品製造のスケールアップにおける真のボトルネックは、製造能力ではなく需要予測にある
多くのバイオ医薬品は、大規模なステンレス設備を必要とするほどの生産量には至りません。
本当に難しいのは、設備を十分に用意することではなく、「いつ」「どれだけ」必要になるのかを正しく見極めることです。
そのため今、注目されているのがスケールの柔軟性です。
需要の変化に合わせて調整できる製造戦略こそが、バイオ医薬品製造における新たな競争力になりつつあります。
その理由を、これから詳しくご紹介します。
16 minute read

ブログ
経口固形製剤(OSD)開発において、後期開発を成功に導くための実践的アプローチ
データに基づいた開発戦略とリスク管理、そして信頼できるCDMOとの連携により、経口固形製剤(OSD)の後期開発スケールアップを、無理なく確実に成功へ導く方法を分かりやすく解説します。
11 minute read

ブログ
創薬を加速する“戦略的インテグレーション”とは何か: CPHI Frankfurt で語られたリーダーの洞察
スピード、コスト、規制対応——そのすべてが同時に問われる時代。
CPHI Frankfurt 2025 の講演で、Jennifer Cannon(President of Commercial Operations, Thermo Fisher Scientific)は、投資家からの期待の高まり、資金調達サイクルの短期化、規制要件の複雑化という現実を背景に、
**「価値は、どこで、どのように生まれるのか」**という本質的な問いを投げかけました。
単なるスピード競争では、もはや差別化はできない。
いま、医薬品開発における価値創出の定義そのものが、再設計されつつあります。
10 minute read

ブログ
OSD開発でつまずかないために:初期製剤設計が規制対応を左右する理由
経口固形製剤(OSD)開発における初期の製剤設計の選択は、プログラム全体の行方を大きく左右します。
バイオアベイラビリティや安定性、あるいは規制ドキュメントに関する問題は、往々にして後工程で顕在化し、高コストな遅延を招きます。
製剤戦略を初期段階からスケーラビリティと規制対応に整合させることが、INDからNDAまでを見据えた確実な開発につながります。
10 minute read

ブログ
初期ステージのバイオベンチャーが知っておくべき、外注戦略の成功と失敗の分岐点
本ブログでは、創薬初期段階における意思決定が開発プログラム全体に与える影響に焦点を当て、アウトソーシング戦略をいかにして競争力のある開発モデルへと進化させるかを解説します。
初期構想から下流工程の実行までを一貫して見据えたアプローチにより、遅延やリスクを最小化し、開発スピードと成功確度を高めるための実践的な視点をご紹介します。
10 minute read

ブログ
アンシラリーサプライ管理から考える治験の規制対応
アンシラリー管理において直面する規制上の課題と、リスクを最小化し、変化する要件へ最適に適応するためのアプローチについて、専門家の視点から解説します。
15 minute read

Blog post
CDMO/CROの統合で実現する、医薬品開発のスピードアップ
研究開発費の高騰や開発期間の長期化など、医薬品開発を取り巻く環境は年々厳しさを増しています。本ブログでは、原薬・製剤開発から治験薬製造、臨床試験、治験薬サプライチェーン管理までを統合的に支援するCDMO/CROアプローチに着目し、開発の複雑化をいかに解消し、効率化とリスク低減を実現できるのかを分かりやすく解説します。研究から上市までのスピードを高めるためのヒントを、ぜひご覧ください。
12 minute read

Blog post
バイオテックの未来を語る
バイオテック産業を形づくる最新トレンドについて、専門家の視点から探ります。イノベーション、サステナビリティ、AI、そして成長を支えるダイナミックな環境など、多角的なテーマを取り上げます。
10 minute read

Five hidden risks in early-phase OSD formulation development
Early-phase oral solid dose development presents a range of hidden risks that can impact long-term success. From API complexity to scalability and regulatory readiness, thoughtful planning can help mitigate setbacks and keep programs on track.
12 minute read
Blog post
臨床試験の成功を加速する最新パッケージング&ラベリング戦略を専門家が解説
革新的な臨床試験用パッケージング&ラベリングソリューションが、どのようにプロセスを効率化し、業務の精度とスピードを高め、規制遵守を確実にしながら臨床試験全体の成功につなげるのか――。
専門家によるインサイトを、ぜひ本ブログでご覧ください。
15 minute read

バイオ医薬品の細胞株開発における科学的アプローチ:安定性と収率改善
バイオ医薬品製造において、細胞株開発は効率性やスケーラビリティ、製品の安定性を左右する重要なプロセスです。
近年進歩している CHO-K1細胞株エンジニアリング により、より高い生産収率、遺伝子の安定性向上、そしてIND申請までの迅速な道筋が実現可能になっています。
当社の最新アプローチは、研究から臨床開発までを加速し、より信頼性の高いバイオ医薬品製造を支援します。
15 minute read

Understanding large molecule drugs
This blog provides a deep dive into large molecule drugs, or biologics, exploring their key characteristics, advantages and challenges, and future in the pharmaceutical industry.
18 minute read

Blog post
コールドチェーン・ロジスティクスの重要な役割:研究室から患者まで、医薬品の品質を守る
本ブログでは、バイオ医薬品業界におけるコールドチェーン・ロジスティクスの重要な役割について解説し、CDMO/CROパートナーが医薬品開発企業とともに、製品の品質と有効性を確保するためにどのように貢献できるのかをご紹介します。
(12 minute read)

ブログ
医薬品開発プロセスの加速を新たに定義する
製薬業界では、必要な治療法を患者に迅速かつ安全に届けるためには、開発過程全体で遅延や複雑さ、リスクを最小限に抑えることが重要です。Thermo Fisher ScientificのAccelerator™ Drug Developmentは、CDMOおよびCROの360°統合ソリューションを提供し、開発に必要なすべてのサービスを一か所で提供します。この統合サービスにより、製薬企業は治療法を患者に届けるまでの時間を大幅に短縮することが可能になります。
16 minute read
ブログ
低分子医薬品とは何か?その開発、製造、そして可能性についての洞察
低分子医薬品の基本から詳しく解説します。開発や製造における主な課題、そして現代医療における将来の可能性について探ります。
16 minute read

ブログ
CPHI 2024からの洞察:柔軟な財務ソリューションで細胞・遺伝子治療開発の高コストを乗り越える
細胞・遺伝子治療の開発者は、重要なプロジェクトを停滞させる可能性のある大きな財務的課題に直面しています。柔軟な財務ソリューションは、コスト管理と治療の進展を支援しています。CPHI 2024 Milanでは、Thermo Fisher Scientificのウイルスベクター、mRNA、細胞治療サービス部門のコマーシャル部門のであるバイスプレジデントであるケリー・ハワードが、Thermo Fisher Financial Solutionsを通じて利用可能な柔軟な選択肢について講演しました。
8 minute read

ブログ
プロセス開発が重要な理由:バイオテクノロジー企業と製薬企業にとっての6つのメリット
このブログでは、医薬品開発と製造におけるプロセス開発の重要な役割について解説しています。さらに、プロセス開発を優先することでスポンサー企業が得られる6つの主なメリットを紹介します。
15 minute read

ブログ
持続可能なAPI開発と製造に向けたグリーンケミストリーの活用
API(医薬品有効成分)の初期開発段階は、リスクや課題が伴うものの、環境に優しい製造方法を取り入れるための重要なタイミングです。この取り組みは、廃棄物を減らし、エネルギーや資源の使用を最小限に抑えるなど、環境への負荷を軽減することを目的としています。また、これにより化合物が臨床試験に進む過程で、大規模かつコスト効率の高い製造プロセスを実現するための土台を築くことができます。
9 minute read

Blog post
医薬品開発の課題に応える: バイオ原薬のCDMOサービスに関するインサイダーの見解
今年のBIO International 2024では、世界中から業界リーダーや顧客が集まり、医薬品開発と製造の最新動向や課題について議論しました。弊社のバイオ原薬部門コマーシャルオペレーション担当バイスプレジデント、メイダー・パリク博士に、バイオ原薬の開発・製造に従事する顧客が直面する一般的な課題と、サーモフィッシャーサイエンティフィックのCDMOサービスがどのようにそれらに対処しているかについて、インサイダーの視点から語ります。
9分で読めます

技術移転パート2:製薬技術移転における戦略的パートナーシップの価値
戦略的なパートナーシップは、技術移転の成功において重要な役割を果たします。これにより、プロセスのリスクを特定して軽減することができ、プロジェクトのスケジュールを守り、技術移転における一般的な課題を克服し、コストの大幅な削減を実現することが可能です。
10分で読みます

技術移転パート1:製薬製造における技術移転の重要な役割
効率的な技術移転は、製薬製造において、製品の品質を守り、知的財産を保護し、コストを管理し、スケールを拡大するために重要です。これにより、企業は新しいチャンスや課題に柔軟に対応でき、競争力を維持し、患者さんへの医薬品供給を途切れることなく続けることが可能になります。
15分で読めます

溶解性およびバイオアベイラビリティ向上のための予測モデリング
製剤開発における低溶解性・低バイオアベイラビリティの課題と、予測モデリングによる解決の可能性をご紹介します。
候補化合物の特性を開発初期に見極め、適切な製剤戦略を導くための新たなアプローチとして、予測モデリングが注目されています。
是非ご一読ください。
15 minute read

Blog post
ウイルスベクターの開発と製造における統合的アプローチの利点の評価
バイオ製薬企業が社内での開発・製造ではなく、ウイルスベクターの開発・製造に豊富な経験を持つ総合的なCROやCDMOと提携を選ぶ理由をご覧ください。
15 minute read

Blog post
ウイルスベクター製品の旅路を理解する: 主な成果物と製造上の考慮事項
遺伝子治療のためのウイルスベクター開発と製造において、CDMOが提供する革新的で統合された即戦力のソリューションを活用するメリットを解説します。バイオ製薬企業がCDMOと提携を選ぶ理由について、詳しくご紹介します。
20 minute read

専門家の視点 デジタル化による臨床試験サプライチェーンの最適化
治験薬がFDAや他国の規制当局から承認を受けるまでの道のりは、第I相から第IV相までの臨床試験を経て、多くのボランティアを対象に安全性と有効性が評価されなくてはなりません。しかし、現実は平均で約7.9%のみが承認を得ることができるという厳しい現実があります。
15 minute read

Blog post
バイオリポジトリをアウトソーシングするメリットとデメリット
バイオリポジトリに関して、バイオファーマ企業はストレージのニーズをインソースすべきか、アウトソースすべきか?このブログでは、そのメリットとデメリットについて説明する
8 minute read
ブログ
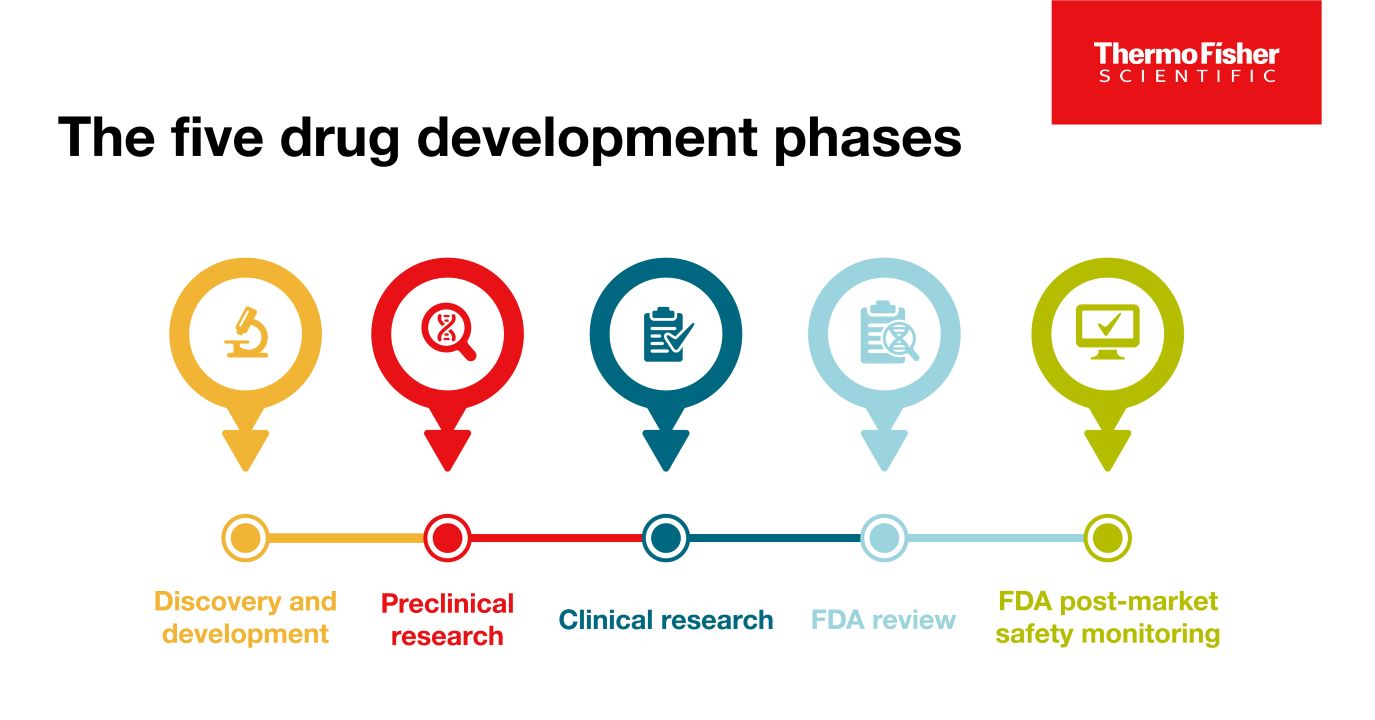
医薬品開発における5つのフェーズ(段階)について
新薬が「成功」とみなされるためには、5つの段階を経る必要があります: 1)発見と開発、2)前臨床研究、3)臨床研究、4)FDA審査、5)安全性監視
9 minute read
ブログ
服薬遵守と正確性:スマートパッケージが臨床試験における品質向上に貢献します
サーモフィッシャーの服薬遵守とバイオマーカー測定の責任者から、スマートパッケージのデータ品質に関する知見と、それを臨床試験にどのように統合するかを学びましょう。
15 minute read

ブログ
CRDMOの興隆:未来の医薬品開発を切り拓く統合アプローチ
CROとCDMOの強力な連携から生まれた「CRDMO」が、新しい時代の扉を開こうとしています。今回、CRDMOとの提携がもたらす5つの魅力的なメリットに焦点を当て、未来の医薬品開発における真の可能性を探ります。
9 minute read

ブログ
CROとCMOとCDMO: 3つの違いについて
CRO、CMO、CDMOは、いずれもバイオテクノロジー企業や製薬企業の医薬品開発・製造をサポートするものですが、それぞれの違いは何でしょうか?
9 minute read

Blog post
CDMOとは? 質の高いCDMOパートナーを探す7つのポイント
製薬企業とCDMO(医薬品開発・製造受託機関)がどのように連携しているか、そしてCDMOパートナーを選ぶ際に最も考慮すべきポイントをご紹介します。
9 minute read

ブログ
ウイルスベクターの商用化(パート2)‐ プロセス検証ライフサイクル
ウイルスベクターの安全性、有効性、品質を確保するためには、さまざまな評価と研究が必要です。これについて詳しく知りたい方は、頑健なウイルスベクタープロセスの検証サイクルをご覧ください。
11 minute read

ブログ
ウイルスベクターの商用化(パート1)‐ 技術移転
ウイルスベクターは、遺伝子治療やワクチンの革新的な開発を可能にし、その需要が急上昇しています。しかし、製造と商用化には高度な科学的専門知識と技術が必要となり、技術移転がキーの役割を担っています。
9 minute read

ブログ
First-in-Human の一般的な技術文書に適切な量の詳細を提供するための重要なヒント
開発の初期段階では、薬剤の特性についてはほとんどわかっていない可能性があります。さらに、試験や治験の後にさらに多くの情報が明らかになるにつれて、医薬品のプロセスや製剤は頻繁に進化します。もっと詳しく知る。
5 分で読めます

ブログ
統合されたビジネスプロセスを通じてデジタル文化を実現する
安定性と経験が鍵となる物理的な作業環境とは対照的に、デジタル ビジネス環境ではイノベーションと接続性に重点が置かれます。
4 分で読めます

ブログ
API をより深く理解する
医薬品原薬 (API) がますます複雑になるにつれて、スケジュールが延長され、予算が急増する可能性がある潜在的な製剤上の問題が生じます。詳細については、このブログをお読みください。
5 分で読めます

ブログ
EU と米国の規制: 細胞治療と遺伝子治療に何が起こるのか?
細胞および遺伝子治療 (CGT) の開発者は現在、臨床試験を経て製品を市場に投入するというさらなる課題に直面しています。詳細については、このブログをお読みください。
7 分で読めます
ブログ
mRNA を成功させるための CDMO の選択: 必要な CDMO の 5 つの特徴
mRNA テクノロジーの有望性は、ワクチンが記録的な速さで市場に到達するなど、新型コロナウイルス感染症のパンデミック中に明確に実証されました。
7 分で読めます
ブログ
mRNA 治療薬のトレンド: パンデミックから学んだ成功への道
ファイザー・ビオンテックとモデルナのメッセンジャーRNAベースの新型コロナウイルス感染症ワクチンが研究室から診療所まで急速に進歩
5 分で読めます

ブログ
ワクチン用のバイアルからプレフィルドシリンジへの移行: 3 つの重要な成功要因
製薬会社がより患者中心になり、注射薬の自己投与が増加し続けるにつれ、プレフィルドシリンジの医薬品市場は成長し、2026 年までに 95 億 3,000 万ドルに達すると予測されています。
4 分で読めます

ブログ
機器認定の 4 段階
前回のブログで説明したように、認定とは、特定の機器、設備、またはシステムが意図した用途に適合し、準備ができていることを文書化した証拠を確立するプロセスです。
3 分で読めます

ブログ
あなたのサプライチェーンは完璧ですか?
応答する前に、ハリケーン、ノーイースター、津波について考えてください。地震、台風、火山の噴火。内乱と戦争。テロ。パンデミックウイルス。
2 分で読めます

ブログ
臨床ラベルの翻訳と規制要件を管理する方法に関する重要なヒント
臨床試験に含まれるすべての国のラベル翻訳と規制要件を常に把握する方法を見つけられたら素晴らしいと思いませんか?
2 分で読めます

ブログ
パッケージングについて考え始める時期が来ましたか?
この見出しが目に留まった場合は、有望な前臨床結果が得られ (おめでとうございます!)、次のステップの計画を考え始めているからかもしれません。
2 分で読めます

ブログ
API を次のレベルに引き上げる: アウトソーシングする前に考慮すべき 3 つのステップ
API 開発のアウトソーシングが一般的になるにつれ、潜在的な開発パートナーとして競合する複数の受託開発製造組織 (CDMO) が台頭すると考えられます。
10 分で読めます

ブログ
OTCノイズを打ち破る
それは秘密ではありません。消費者は、お気に入りの店舗やオンライン小売店で幅広い OTC オプションを利用できます。錠剤やカプセルからシロップに至るまで、OTC ジャングルの中で消費者にはこれまで以上に多くの選択肢があります。
8 分で読めます

ブログ
希少疾病用医薬品の開発を妨げる考慮事項と障害
米国食品医薬品局(FDA)によると、「2020年は、希少疾病用医薬品開発局に提出された希少疾病用医薬品指定および希少小児疾患指定申請の数において、記録的な年となった」とのこと。
6 分で読めます

ブログ
ヨーロッパの規制状況: Brexit 後の有資格者の要件を満たすための重要なアドバイスrequirements
英国(UK)の欧州連合(EU)離脱により、新型コロナウイルス関連の混乱に加えて、欧州の臨床試験サプライチェーンはさらに複雑さを増しました。
4 分で読めます

ブログ
電子ラベルを採用する時期が来ていますか?新しい EU 臨床試験規則に基づくラベル表示ソリューションの可能性
新しい EU 臨床試験規制 (CTR) は、臨床試験の管理を簡素化し、欧州で事業を展開する製薬会社にとってより歓迎的な環境を作り出すことを目的としています。
5 分で読めます
ブログ
PPQ(プロセス製造適格性評価)の複雑さを乗り越える
メソッドの認定は、プロセス性能認定 (PPQ) の前に非常に重要です。メソッドのパフォーマンス特性を早期に評価することは、メソッドの検証と、精度、精度、直線性などのパラメーターに関係するため、非常に重要です。
5 分で読めます

ブログ
連続製造: OSD 医薬品を生産する効率的な方法
1913 年にヘンリー フォードがミシガン州ハイランド パークで製造慣行に革命を起こしたとき、彼の主な目標は単純でした。つまり、最も効率的かつ費用対効果の高い方法で可能な限り最高の製品を作るということでした。フォードは、従業員やテクノロジーがよりスマートに働き、原材料の無駄を削減できるように製造の「フロー」を改善することに重点を置き、製造原則を永遠に変えました。
6 分で読めます

ブログ
新型コロナウイルス感染症の希望の光: ワクチン開発の加速
ワクチン開発は長いプロセスであり、費用がかかり、人員の減少が多く、認可されたワクチンをすべての人に届けるには、候補を複数回繰り返す必要があります。パンデミックや伝染病に対するワクチン開発にはリスクが伴い、ウイルスの新しい性質により、特定の未知の要因によってワクチン計画が狂う可能性があります。
6 分で読めます

ブログ
分散型臨床試験が新型コロナウイルス感染症の時代にどのように患者中心性を高めるか
新型コロナウイルス感染症により、バイオ医薬品業界でのビジネスのやり方が変化し続けているため、患者の命を改善し救うという、なぜ私たちがやっているのかを見失わないことが重要です。
5 分で読めます

ブログ

ブログ
プレフィルドシリンジ: 考慮されていないかもしれない 3 つの問題点
製薬会社がより患者中心になろうとするにつれ、特定の医薬品がその取り組みをサポートするために最前線に立つようになりました。
5 分で読めます
ブログ
細胞および遺伝子治療の規制をナビゲートする: 貴社の CDMO はどのように適合しますか?
大規模なバイオテクノロジー企業であっても、新興の新興バイオテクノロジー企業であっても、多くの企業は、規制当局への申請を適切にサポートするための社内リソースや専門知識が不足していると感じています。
7 分で読めます

ブログ
真のバイオ医薬品製造の専門家である CDMO を選択する重要性
バイオプロダクションの業界では CDMO の数が増加しているため、新興のバイオ医薬品企業にとって、どの CDMO が自社に適しているかを判断するのは困難になる可能性があります
8 分で読めます