バイオ医薬品の分析法・処方開発サービス
データに基づく成果により、各ステップを確実に推進
有効性の確認から実臨床での採用確保まで、バイオ医薬品の成功には、治療上の必要条件を的確に満たす頑健性の高い分析法と原薬/製剤処方の構築が欠かせません。
分析法としては、タンパク質/抗体の同一性の確認、力価の評価、目的物質/工程由来不純物の検出、翻訳後修飾(PTM)の特性解析といった主要試験が挙げられます。高度な品質特性モニタリングにAnalytical Target Profile(目標品質プロファイル:ATP)を組み込むことにより、分析法と各社の治療目標および規制要件との整合性が確保され、工程管理戦略のための明確なフレームワークを構築することが可能です。
バイオ医薬品の原薬開発では処方も重要です。患者ニーズを満たす原薬/製剤処方を開発し、イオン強度、pH、せん断力、界面活性剤などの重要特性を最適化することにより、安定性を高め、保存条件を改善し、配送の選択肢を広げることが可能です。製品の安定性は極めて重要です。安定性に基づく有効期間の設定および長期的な有効性の確認により、製薬業界で不可欠な、性能の一貫性と患者さんの安全を確保できるからです。
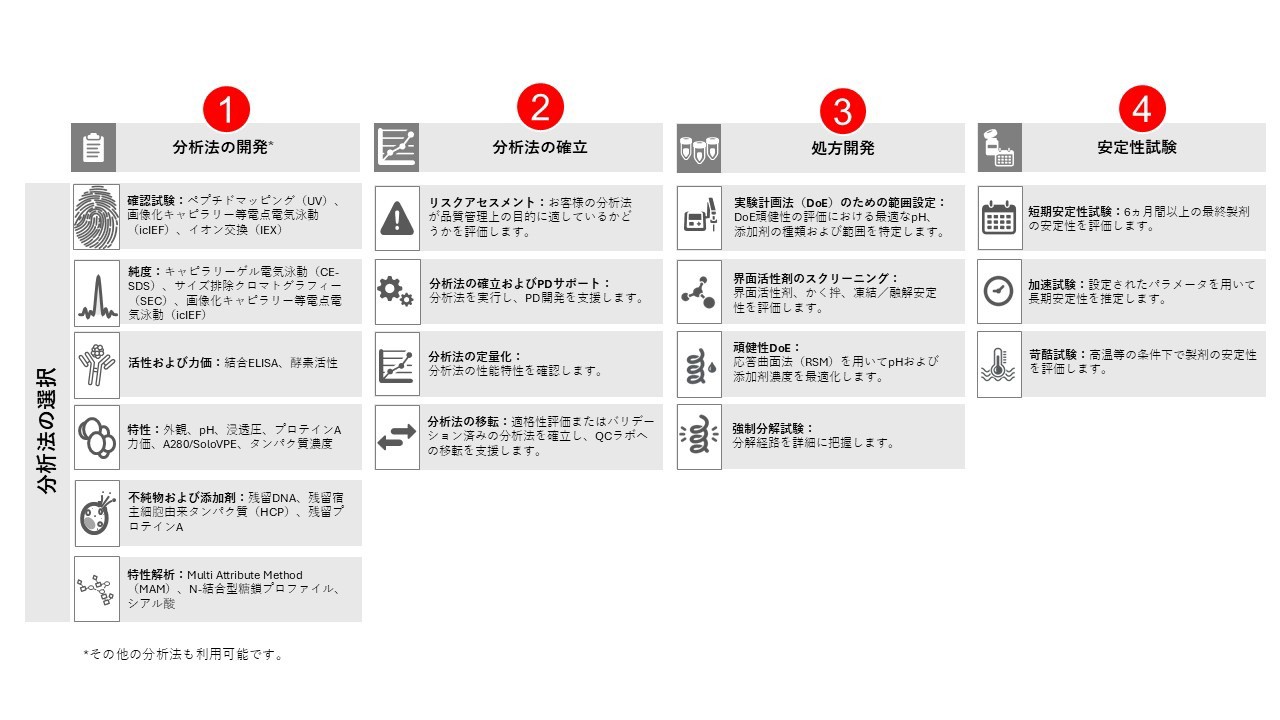
3つの重要要素:
目的物質の確実な同一性確認
バイアル中の目的物質の同一性を確認します。確認試験方法のうち、複数の特性を同時に分析するMulti Attribute Method(MAM)を用いて、アミノ酸配列を決定し、脱アミド化、酸化、糖鎖付加などのPTMを特定します。
経験豊富な処方開発チーム
数多くのバイオ医薬品を作り上げてきた業界トップクラスの実績を誇るチームが、患者さんが必要とする濃度で各分子に最適な処方の構築を支援いたします。
早期の安定性試験によるスケジュールリスクの排除
安定性試験は、最適な保存条件を設定し、目的とする剤形でのバイオ医薬品製剤の配送を確保し、製品の出荷や臨床試験に必要とされる有効期間を早期に把握する上で極めて重要です。
画期的バイオ医薬品のコンセプト段階から製品実現までの道のりに全力で取り組むエキスパートをご紹介します。

Elena Gontarz, PhD, St. Louis, Missouri, USA
生化学(biochemistry)分野で博士号を有し、製薬企業向けバイオ医薬品の開発において10年以上の経験を持つGontarz博士は、グローバルな分析開発およびプロセス開発、ならびに製剤科学における当社の第一人者です。現在はサイエンティフィック/テクニカルアフェアーズチームの責任者として、CMCサポートを統括し、フェーズIから商用製造に至るまでのバイオ医薬品プログラムをリードしています。
Gontarz博士とのミーティングを通じて、分析法ライフサイクル開発、細胞株開発、プロセス開発、技術移管、ならびに後期フェーズの商業化に関する当社の取り組みについて、ぜひ詳しくご確認ください。

Palak Patel, St. Louis, Missouri, USA
初期段階のバイオ医薬品開発において5年以上の経験を有し、製薬企業向けに革新的なソリューションを提供してきたPalakは、バイオ医薬品における細胞株および細胞培養開発分野のサイエンティフィック/テクニカルアフェアーズの分野専門家の一人です。
Palakとのミーティングを通じて、当社の初期段階バイオ医薬品ソリューションが、貴社のバイオ医薬品をより迅速に患者さんへ届けるためにどのように貢献できるかをご確認ください。

Otto P.J. Jurrius, Groningen, Netherlands
バイオテクノロジー分野の修士号を有し、20年以上にわたるバイオ医薬品業界での経験を持つOttoは、オランダ・フローニンゲンにあるサーモフィッシャーサイエンティフィックのバイオ医薬品製造拠点において、ジェネラルマネージャーを務めています。Ottoは、バイオ医薬品開発から治験および商用製造に至るまで、プロジェクトマネジメント、製造、エンジニアリング、ならびに拠点全体のマネジメントを統括しています。
Ottoとのミーティングを通じて、当社が提供する革新的な治験および商用製造能力について、ぜひ詳しくご確認ください。

Erica Byerley, Lengnau, Switzerland
化学工学(Chemical Engeering)および生命科学の両分野で学位を有し、8年以上にわたる実務経験を持つEricaは、シングルユース技術、技術移管、プロセス設計、ならびにバイオ医薬品開発から治験製造に至るまでのオペレーショナル レディネスにおける当社の第一人者です。現在、スイス・レンナウ(Lengnau)に新設された最先端施設において、グローバルな技術移管エンジニアリングチームを率いています。
Ericaとのミーティングを通じて、バイオ医薬品開発を加速させる革新的なシングルユースバイオリアクターや、最適化されたエンジニアリング設計について、ぜひ詳しくご確認ください。

Kym Baker, PhD, Brisbane, Australia
免疫ワクチン開発分野で博士号を有し、製薬企業向けのバイオ医薬品の開発および製造において30年以上の経験を持つKymは、これまでに400品目を超えるバイオ医薬品プロジェクトに携わり、そのうち10品目を製品上市まで導いてきました。現在は、オーストラリア・ブリスベンに拠点を置く、受賞歴を有し世界的に規制当局の承認を受けた当社のバイオ医薬品製造施設を率い、フェーズIから商用製造に至るまで、幅広いクライアントプログラムを支援しています。
Kymとのミーティングを通じて、技術移管から治験段階、後期フェーズの商業化および製造に至るまで、製品ライフサイクル全体をどのように支援できるか、またオーストラリアのR&D税額控除制度や治験届出制度(Clinical Trial Notification:CTN)を活用して、初期フェーズの製品をいかに迅速に市場投入へと導けるかについて、ぜひご確認ください。
Featured resources