各種資料&最新情報
カタログ・ウェビナー等 / 製造拠点 / イベント情報
サーモフィッシャーサイエンティフィックの各領域エキスパートのほか、医薬品製造・治験業界の技術・科学エキスパートと協力し、各種ホワイトペーパー、報告、ウェビナーなどをご用意しました。分子から医薬品までの開発プロセスの円滑な推進にご活用ください。
メニューボタンを使って検索を絞り込んでください。下のフィルターを使って、カテゴリーや領域エキスパート、内容別にライブラリ全体を検索することもできます。
資料のダウンロードにあたっては、登録フォームへの入力をお願いする場合があります。
質問はございませんか?お問い合わせは、こちらまでお気軽にご連絡ください。

The science of cell line development for biologics: Improving stability and yield
Cell line development is critical to biologics manufacturing, influencing efficiency, scalability, and product stability. Advances in CHO-K1 cell line engineering, are driving higher yields, improved gene stability, and faster IND submission pathways.
15 minute read

イベント
BIO 医薬 EXPO 2025 (Interphex Japan)
2025年7月9日~11日に東京ビッグサイトで開催させるInterphex Japan 2025 (BIO医薬EXPO) に出展いたします。 会場にお越しの際は是非弊社ブースにお立ち寄りください。

イベント

Understanding large molecule drugs
This blog provides a deep dive into large molecule drugs, or biologics, exploring their key characteristics, advantages and challenges, and future in the pharmaceutical industry.
18 minute read
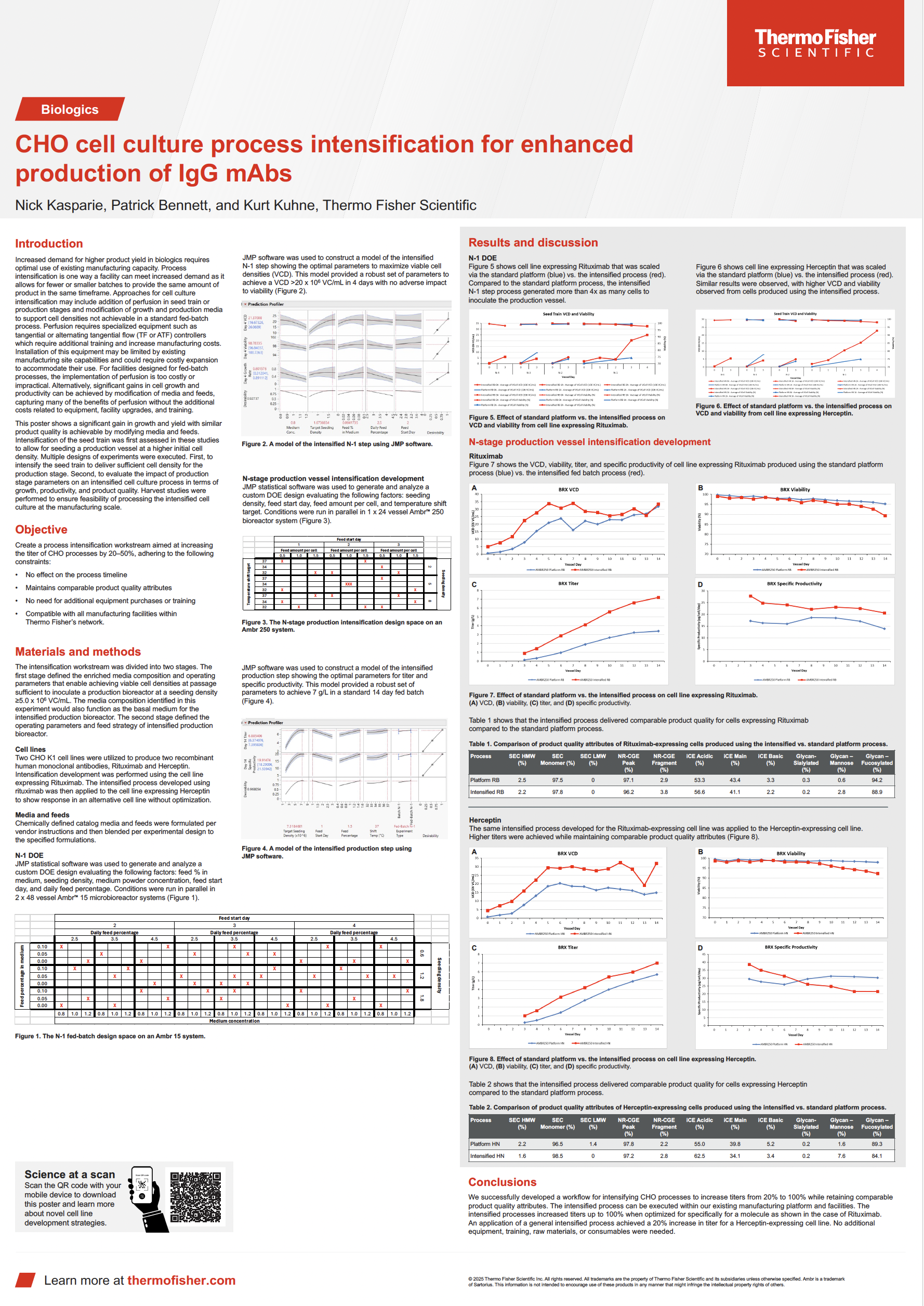
CHO-K1細胞培養プロセスの最適化によるIgGモノクローナル抗体生産性向上
ケーススタディをダウンロードして、当社の科学者がCHO-K1細胞株を活用し、既存の製造プラットフォームと設備を最大限に生かし、品質を損なうことなく、力価を80%向上させた事例をご覧ください。

Webinar
Assessing the application of standardized processes in cell and gene therapy development and manufacturing
This webinar features experts in cell and gene therapy (CGT) development, regulatory affairs, and CMC strategy, offering guidance on assessing the risks and rewards of standardized processes.

Partnership-driven value in drug development: Compelling insights from new research
Partnering with a single vendor for comprehensive drug development, manufacturing, research, and clinical supply services can accelerate trial starts and substantially reduce development costs. New research by the Tufts Center for the Study of Drug Development analyzed the impact of integrated service models on oncology drug programs and showed significant reductions in development timelines across clinical phases while improving cost efficiency.
15 minute read
ホワイトペーパー
組換えAAV(アデノ随伴ウイルス)製造プラットフォームの現状評価
ウイルスベクターを活用した治療法の可能性を最大限に引き出すためには、組換えアデノ随伴ウイルス(AAV)ベクターのための信頼性の高い製造プラットフォームが必要不可欠です。

ブログ
CPHI 2024からの洞察:柔軟な財務ソリューションで細胞・遺伝子治療開発の高コストを乗り越える
細胞・遺伝子治療の開発者は、重要なプロジェクトを停滞させる可能性のある大きな財務的課題に直面しています。柔軟な財務ソリューションは、コスト管理と治療の進展を支援しています。CPHI 2024 Milanでは、Thermo Fisher Scientificのウイルスベクター、mRNA、細胞治療サービス部門のコマーシャル部門のであるバイスプレジデントであるケリー・ハワードが、Thermo Fisher Financial Solutionsを通じて利用可能な柔軟な選択肢について講演しました。
8 minute read

ブログ
CPHI 2024からの洞察:戦略的なCDMOおよびCROパートナーシップによる医薬品開発の加速
製薬およびバイオテクノロジー企業は、競争の激化、厳格な規制、サプライチェーンの複雑化といった課題に直面しています。CPHI Milan 2024でThermo Fisher Scientificのコマーシャル部門プレジデントであるジェニファー・キャノンは、CDMOとCROサービスを組み合わせた統合型アウトソーシングソリューションが、さまざまな治療モダリティにおいて開発プロセスを最適化し、コスト削減を実現する方法について解説します。
12 minute read

ブログ
医薬品開発プロセスの加速を新たに定義する
製薬業界では、必要な治療法を患者に迅速かつ安全に届けるためには、開発過程全体で遅延や複雑さ、リスクを最小限に抑えることが重要です。Thermo Fisher ScientificのAccelerator™ Drug Developmentは、CDMOおよびCROの360°統合ソリューションを提供し、開発に必要なすべてのサービスを一か所で提供します。この統合サービスにより、製薬企業は治療法を患者に届けるまでの時間を大幅に短縮することが可能になります。
16 minute read
記事
mRNA製品の複雑な規制環境を乗り越える
この記事では、mRNA製品における複雑な規制環境に対応するためのベストプラクティスを紹介し、CDMOとの提携がどのように安心感を提供するかを解説します。

ウェビナー
柔軟で効率的なRapid Development Framework™を活用した細胞および遺伝子治療の開発と製造の加速
Rapid Development Framework™は、プロセスと分析の分野で開発と製造のスケジュールを効率化し、各製品の個別ニーズに柔軟に対応することが可能です。このフレームワークがどのように医薬品開発を加速するのか、ぜひ学んでください。

Event
Tradeshow
Advanced Therapies Week 2025
Visit booth #541 at Advanced Therapies Week 2025 from January 20-23 in Dallas, Texas, to discover our CDMO services and solutions for advanced therapies, including cell and gene therapies.
記事
遺伝子治療の未来を拓く:初期革新から商業成功まで、すべての段階でのウイルスベクターパートナー
この記事では、遺伝子治療の最前線に立つ2つの企業、NysnoBio社とbluebird bio社が直面するパートナーシップのニーズを深掘りします。異なる開発フェーズにある両社が、革新的な治療法を患者に届けるためにどのように最適なパートナーシップを築き、成功へと導いたのか、具体的な事例を通じて明らかにします。この記事を通じて、遺伝子治療開発の舞台裏と、CDMOとの戦略的協力の重要性をご覧ください。

技術移転パート2:製薬技術移転における戦略的パートナーシップの価値
戦略的なパートナーシップは、技術移転の成功において重要な役割を果たします。これにより、プロセスのリスクを特定して軽減することができ、プロジェクトのスケジュールを守り、技術移転における一般的な課題を克服し、コストの大幅な削減を実現することが可能です。
10分で読みます

技術移転パート1:製薬製造における技術移転の重要な役割
効率的な技術移転は、製薬製造において、製品の品質を守り、知的財産を保護し、コストを管理し、スケールを拡大するために重要です。これにより、企業は新しいチャンスや課題に柔軟に対応でき、競争力を維持し、患者さんへの医薬品供給を途切れることなく続けることが可能になります。
15分で読めます

Event
Conference and exhibition
ISPE Singapore 2024
Join Thermo Fisher Scientific at ISPE Singapore 2024 from August 29-30 to explore our CDMO services and solutions in APAC and beyond. Visit our team at booth #244 or schedule a private 1:1 meeting now.
ファクトシート
mRNA開発・製造CDMOサービス紹介
新しいワクチンや遺伝子治療の開発を含むmRNA治療薬の出現は、重要な原材料や技術的専門知識へのアクセスに市場の制約を生み出しています。
mRNA治療法の出現により、新しいワクチンや遺伝子治療の開発が進む中、重要な原材料や技術的専門知識へのアクセスに市場の制約が生じています。サーモフィッシャーのmRNAのCDMOサービスをご紹介します。

Fact sheet
トランスレーショナルサービスの紹介
トランスレーショナル・リサーチ・サービスを通じて、サーモフィッシャーの学際的な科学専門家チームは、先端治療薬の開発者にエンド・ツー・エンドのサポートを提供し、関連資料を作成し、創薬から臨床段階の製造へのシームレスな移行を支援します。

Blog post
ウイルスベクター製品の旅路を理解する: 主な成果物と製造上の考慮事項
遺伝子治療のためのウイルスベクター開発と製造において、CDMOが提供する革新的で統合された即戦力のソリューションを活用するメリットを解説します。バイオ製薬企業がCDMOと提携を選ぶ理由について、詳しくご紹介します。
20 minute read

Blog post
ウイルスベクターの開発と製造における統合的アプローチの利点の評価
バイオ製薬企業が社内での開発・製造ではなく、ウイルスベクターの開発・製造に豊富な経験を持つ総合的なCROやCDMOと提携を選ぶ理由をご覧ください。
15 minute read

Webinar
~ウィルスベクターCDMO最前線~ グローバルIND成功の鍵 : 前臨床開発からGMP製造までの一貫戦略
ウィルスベクターのグローバルIND成功に向けた 前臨床開発からGMP製造までの一貫戦略について、トランスレーショナルサービスから開発・商用生産に至るまで、サーモフィッシャーがどのようにサポートすることが可能か、ご説明いたします。(CPhI Japan 2024にて発表した内容)
記事
先端医療医薬品(細胞・遺伝子治療、mRNA)の開発の課題と解決に向けたヒントを探る
"先端医療医薬品(細胞・遺伝子治療、mRNA)の開発の課題と解決に向けたヒントを探る 細胞・遺伝子治療やmRNA技術の開発における課題にも関わらず、このセクターには大きな成長の可能性があり、パセオンはCDMO分野で技術力の向上に向けた積極的な投資を行っており、開発の課題と解決に向けたヒントについてまとめた記事です。"

Infographic
細胞・遺伝子治療および先端医療医薬品の規制パスウェイ
細胞・遺伝子治療は急成長し、患者に治癒の可能性を提供しています。開発者は迅速な進展と新たな課題に直面しており、成熟する領域では規制対応のために規制当局と緊密な連携が必要です。この資料では、規制対応の成功に向けた3つのヒントを紹介します。

インフォグラフィック
最新のパセオンCDMOサービスアップデート
新規化合物は、人々の人生を変え、未来を形作る可能性を持っています。その医薬品の可能性を実現するには、信頼できるパートナーが必要です。この資料では、世界中のお客様のプロジェクトの成功に貢献してきたパセオンのCDMOサービスと実績についてご紹介します。

ビデオ
種細胞療法と自家細胞療法の現在と未来を探る:科学・製造・規制について
このラウンドテーブルでは、臨床と商業の専門家が同種細胞療法と自家細胞療法にまつわる複雑な動向を解説し、業界の現状と未来についての洞察を提供します。製造とロジスティクス、規制の状況とCMC要件、標準化の役割など、具体的なトピックに焦点を当てています。
記事
医薬品開発を促進する調和した戦略:初期段階と後期段階のプロセスの統一
こちらの記事ではサーモフィッシャーサイエンティフィック社が開発したGMPプラットフォームをベースに、創薬研究向けのAAVおよびLVベクターの製造において調和された合理的な手法を提案しています。技術とプロセスが一体化し、現代の要件に対応したアプローチを詳しく解説しています。

インフォグラフィック
細胞療法製造ワークフロー
遺伝子組換え細胞治療のワークフローと、プラスミド製造からコールドチェーン・ロジスティクスまでの各ステップにおける重要なポイントについてご紹介します。こちらの資料をご覧ください。
ファクトシート
ウイルスベクター開発・製造サービス
サーモフィッシャーサイエンティフィックは、ウイルスベクター製品の開発・製造において20年以上の比類ない経験を有しており、エンドツーエンドの包括的なサービスを提供しています。詳細をご覧ください。

ファクトシート
毒性試験用ウイルスベクターサービス
毒性試験は、IND前の規制要件をサポートし、医薬品候補のリスク・ベネフィット比を評価するために極めて重要です。当社のDirect-to-Toxicologyウイルスベクター・サービス・プログラムは、アデノ随伴ウイルス(AAV)およびレンチウイルス(LV)の製造プロセスを通じて毒性学的材料へのルートを迅速化し、最短6ヶ月で完成させます。

ブログ
mRNA 治療薬のトレンド: パンデミックから学んだ成功への道
ファイザー・ビオンテックとモデルナのメッセンジャーRNAベースの新型コロナウイルス感染症ワクチンが研究室から診療所まで急速に進歩
5 分で読めます
ブログ
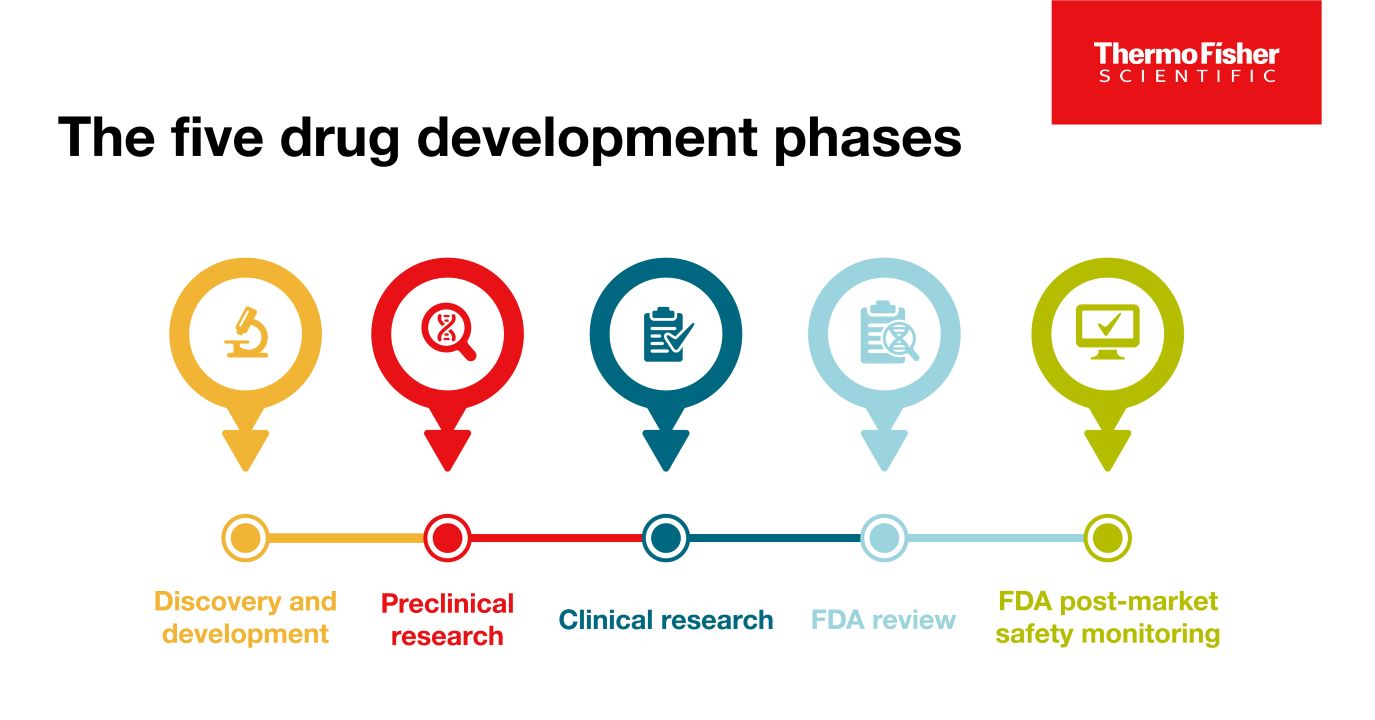
医薬品開発における5つのフェーズ(段階)について
新薬が「成功」とみなされるためには、5つの段階を経る必要があります: 1)発見と開発、2)前臨床研究、3)臨床研究、4)FDA審査、5)安全性監視
9 minute read

ブログ
CROとCMOとCDMO: 3つの違いについて
CRO、CMO、CDMOは、いずれもバイオテクノロジー企業や製薬企業の医薬品開発・製造をサポートするものですが、それぞれの違いは何でしょうか?
9 minute read

ブログ
ウイルスベクターの商用化(パート2)‐ プロセス検証ライフサイクル
ウイルスベクターの安全性、有効性、品質を確保するためには、さまざまな評価と研究が必要です。これについて詳しく知りたい方は、頑健なウイルスベクタープロセスの検証サイクルをご覧ください。
11 minute read

ブログ
ウイルスベクターの商用化(パート1)‐ 技術移転
ウイルスベクターは、遺伝子治療やワクチンの革新的な開発を可能にし、その需要が急上昇しています。しかし、製造と商用化には高度な科学的専門知識と技術が必要となり、技術移転がキーの役割を担っています。
9 minute read

オンデマンド ウェビナー
一貫性あるCRO CDMO パートナーシップで細胞療法の患者サポートを最適化
このオンデマンド・ウェビナーでは、一貫したCRO/CDMOパートナーシップがどのように業界の課題を緩和し、開発から製造までのプロセスを加速するかに焦点を当てます

ファクトシート
cGMP製造に向けたPOC試験のサポートサービス
当社ではトランスレーショナル・リサーチ・サービスを通じて、製薬会社向けにエンドツーエンドでサポートを提供します。先進治療法の開発者に対して、関連資料を作成し、発見から臨床段階の製造へのスムーズな移行をお手伝いします。

Webinar
mRNA製品の商用化における業界の課題に迫る
COVID-19パンデミックでのmRNAベースワクチンの急速な開発・承認により、mRNA技術への新たな注目が高まり、科学者たちは腫瘍学、HIV、希少疾患、そして個別化医療などの新しい応用分野を模索しています。mRNAの生産速度と柔軟性は素晴らしいが、その潜在能力を最大限に引き出し、さらなる発展を遂げるためには、業界のいくつかの課題に果敢に取り組む必要があります。詳細はこちらをご覧ください

Infographic
mRNA 製造ワークフロー
このインフォグラフィックでは、mRNA製造の各ステップを詳しく解説し、サーモフィッシャーサイエンティフィックの柔軟なアプローチによって、mRNA製品をより速やかに臨床と市場に提供する方法についてご紹介します

Blog post
CDMOとは? 質の高いCDMOパートナーを探す7つのポイント
製薬企業とCDMO(医薬品開発・製造受託機関)がどのように連携しているか、そしてCDMOパートナーを選ぶ際に最も考慮すべきポイントをご紹介します。
9 minute read

オンデマンド ウェビナー
商用化に向けたウイルスベクター製造の準備
遺伝子治療用ベクターは急速に商業化されつつあるため、成功のためには商業化への準備が不可欠です。こちらのウェビナーでは、商業化に向けたウイルスベクターの準備に関する当社の能力とアプローチについてご紹介しています。

視聴する
遺伝子治療の進化:統合的なアプローチがもたらすメリット
遺伝子治療用ウイルスベクターの商業化には、規制遵守、デザイン、仕様、サプライチェーン戦略の緻密な検討が欠かせません。このウェビナーでは、遺伝子治療用ウイルスベクターの開発と商業化において、ハードルを乗り越え、プロジェクトを効果的に進める方法を解説します。

ホワイトペーパー
品質の全体的な理解を通じて、CDMOとのパートナーシップを強化する
CDMO品質の重要な指標を詳しく掘り下げ、継続的な改善を促進し、協力を強化し、信頼を築くためのツールとベストプラクティスをご紹介します。

ブログ
CRDMOの興隆:未来の医薬品開発を切り拓く統合アプローチ
CROとCDMOの強力な連携から生まれた「CRDMO」が、新しい時代の扉を開こうとしています。今回、CRDMOとの提携がもたらす5つの魅力的なメリットに焦点を当て、未来の医薬品開発における真の可能性を探ります。
9 minute read

オンデマンド ウェビナー
遺伝子治療(ウィルスベクター)の開発と製造における統合的アプローチの利点
「グローバルCDMOの戦略的な活用法」 遺伝子治療用ウイルスベクターの商業化には、規制遵守、設計、仕様、サプライチェーン戦略の慎重な検討が必要です。

インフォグラフィック

インフォグラフィック
FIH書類作成をきちんと行うことは重要です。こちらの資料では、共通技術文書(CTD)のフェーズに適した化学、製造、および管理(CMC)モジュールを作成する際に有益なチェックリストを提供いたします。
FIH書類作成をきちんと行うことは重要です。こちらの資料では、共通技術文書(CTD)のフェーズに適した化学、製造、および管理(CMC)モジュールを作成する際に有益なチェックリストを提供いたします。

eBook
米国とEUの細胞・遺伝子治療薬: 差別化できる5つの主要なポイント
「細胞・遺伝子治療薬(CGT)やその他の複雑な生物製剤の場合、米国とEUの規制プロセスは、単に管轄の監督だけでなく、様々な点で異なります。

eBook
製薬・バイオテクノロジー産業における持続可能性について
現在、我々は気候変動の転換期にあり、無駄にする時間は残されていません。私たちが互いに持続可能な道を歩んでいくためには、コラボレーションが不可欠です。

ファクトシート
遺伝子・細胞治療薬に関するCDMOサービスおよび治験薬サプライチェーンソリューション&コールドチェーンサービスの紹介
サーモフィッシャーが提供する最新の細胞治療薬、遺伝子治療、ウィルスベクター、プラスミドDNA,mRNAのCDMOサービス、および、治験薬サプライチェーンソリューションやゴールドチェーンサービスについて分かりやすくご紹介いたします。

動画
Vectoring In — Viral Vector Video Series
Preparing cell and gene therapies for regulatory submission
When preparing to ramp up late stage manufacturing for commercialization, understanding key critical to quality parameters will help prepare your therapy for regulatory submission.
記事
サプライチェーンロジスティクスにおける商用化に向けた準備について(細胞・遺伝子治療)
細胞・遺伝子治療市場の急速な拡大に伴い、イノベーターは、治療を必要とする患者に治療薬を安全かつ効率的に配送するための信頼できるサプライチェーンソリューションを必要としています。
ブログ
mRNA を成功させるための CDMO の選択: 必要な CDMO の 5 つの特徴
mRNA テクノロジーの有望性は、ワクチンが記録的な速さで市場に到達するなど、新型コロナウイルス感染症のパンデミック中に明確に実証されました。
7 分で読めます

ブログ
EU と米国の規制: 細胞治療と遺伝子治療に何が起こるのか?
細胞および遺伝子治療 (CGT) の開発者は現在、臨床試験を経て製品を市場に投入するというさらなる課題に直面しています。詳細については、このブログをお読みください。
7 分で読めます

ブログ
統合されたビジネスプロセスを通じてデジタル文化を実現する
安定性と経験が鍵となる物理的な作業環境とは対照的に、デジタル ビジネス環境ではイノベーションと接続性に重点が置かれます。
4 分で読めます

ケーススタディ
COVID-19ワクチンの世界的な需要に応えるための弊社の取り組みについて
この2年間、世界を震撼させたCOVID-19の世界的に大流行しています。公衆衛生と経済危機の両方を引き起こしたこのパンデミックは、第二次世界大戦終結後、文明に対する最大の脅威と言われています。

ホワイトペーパー
細胞治療および遺伝子治療製品のCMC規制の状況を理解する
すべてのバイオテクノロジー製品と同様に、命を救う医薬品の早期の上市は、規制当局の査察に対する準備ができていなければ、遅れる可能性があります。

ホワイトペーパー
細胞・遺伝子治療製品のプロセスバリデーションの複雑さを克服する
複雑な細胞・遺伝子治療(CGT)製品では、開発・商業生産ライフサイクル全体にわたって、頑健なプロセスに関する知識を蓄積することが求められます。

オンデマンド ウェビナー
細胞・遺伝子治療製品を商業化するための柔軟な規制対応とCMCにおいて考慮すべき事項
近年、細胞治療と遺伝子治療のパイプラインは急速に拡大しており、アンメットメディカルニーズの高い疾患を治療する大きな可能性を秘めています。

オンデマンド ウェビナー
ウイルスベクターの生産能力・製造技術を構築し、遺伝子治療の可能性を実現する
こちらのセッションでは、サーモフィッシャーサイエンティフィック、Viral Vector ServicesのVice President兼General ManagerであるChris Murphyが、ウイルスベクター製品の上市における課題と機会について解説するとともに、サーモフィッシャーにおける遺伝子治療の可能性実現のための生産能力・製造技術の構築方法についてご紹介します。

オンデマンド ウェビナー
mRNAワクチンのトレンド、技術、サプライチェーンについて
過去10年間でH1N1インフルエンザ、Sars-Cov、EbolaおよびMERSの発生は、パンデミックおよびエピデミックへの戦略的アプローチと対応についての継続的な会話が行われてきました。

オンデマンド ウェビナー
適切な意思決定による早期上市の実現
バイオ医薬品の開発成功には、バリデーションから上市までの道のりに伴うリスクや要件、課題の理解が不可欠です。資源や技術力・専門知識が不足している場合など、初期開発において重要な意思決定を適切に下すことは簡単ではありません。

オンデマンド ウェビナー
細胞・遺伝子治療の商業化を成功させるための、進化する規制環境への対応
細胞・遺伝子治療は、臨床試験を経て、商業化に向けて急速に進展しています。その結果、規制当局は、開発のペースをサポートするためのガイダンスを提供するために、迅速に対応しなければならなくなりました。

オンデマンド ウェビナー
細胞治療製造のためのCDMOパートナーを選択する際の主な考慮点
細胞・遺伝子治療市場は、加速する市場承認、記録的な投資、強固な治療パイプライン、良好な臨床結果などを経験しており、これらすべてがスピード、規制ノウハウ、製造技術の革新の必要性を後押ししています。

オンデマンド ウェビナー
先端治療応用で使用するプラスミドDNAの製造戦略
「細胞・遺伝子治療市場は急速な投資とIND申請の増加を続けており、これらの画期的な治療法の開発に用いられる重要な原材料について、規制ガイドラインの適切な適用と製造戦略に関する新たな疑問が生じています。

ファクトシート
CTX ソリューション ファクトシート
細胞および遺伝子治療市場は、市場承認の機会の加速、記録的な投資、強力な治療パイプライン、良好な臨床結果を経験しており、これらすべてがスピード、規制上のノウハウ、製造技術の革新の必要性を促進しています。

ファクトシート
先進的な治療サプライチェーンソリューション
サーモフィッシャーサイエンティフィックは、カスタマイズされたパッケージングやラベリングから、患者サンプル、薬剤、細胞株の安全なコールドチェーン保管までのサービスを提供しています。
インフォグラフィック

ホワイトペーパー
技術移転。成功の最大化とリスク軽減のためのベストプラクティス
スケールアップのための製造拠点の変更であれ、開発から製造への移行であれ、技術移転はすべての医薬品が市場投入されるまでに通過しなければならない重要なプロセスです。 技術移転を成功させることで、生産性と効率の向上、プログラムコストの削減、規制対応力の最適化、そして市場投入までの時間の短縮を実現することができます。こちらの資料では、よくある落とし穴、ベストプラクティス、次の技術移転を成功させるための重要な要素について説明しています

ブログ
Panteli Theocharous
Global Vice President, Cell and Gene Therapy Strategy lead at PPD, part of Thermo Fisher Scientific.
Scientific Expertise:
- Cell and Gene therapy
- Cancer Immunotherapy expert
Focus Area
Stem Cell Transplantation,
Cell and Gene Therapies
JACIE – The
Joint Accreditation Committee of the International Society for Cellular Therapy (ISCT) and
the European Group for Blood and Marrow Transplantation (EBMT) Inspector
Credentials
M.S. in Applied Clinical Hematology ,University of London
Cancer medicine related higher degrees, University of London

ブログ
Richard Snyder, PhD
Vice President, Science and Technology
Scientific Expertise:
- Oral solid dosage forms, tablets, hard shell capsules, and softgels
- Virus biology
- Viral vector development
- cGMP viral vector manufacturing & analytical technologies
- Viral vector mediated gene transfer
- Development of novel viral vector-based human gene therapies
Focus Area
Viral Vector Services
Credentials
Post-doctoral fellow at Johns Hopkins University School of Medicine
Doctor of Philosophy in microbiology from The State University of New York at Stony Brook
Bachelor’s degree in biology from Washington University in St. Louis

ブログ
Monica Commerford, PhD
Head of Viral Vector Services Regulatory Affairs
Scientific Expertise:
- Cell and gene therapy CMC expert
- Microbiology and molecular genetics
- Microbial control, Product Quality microbiology, and Sterility Assurance for investigational new drug and marketing applications
- Developing, editing and reviewing regulatory submissions, including reviews as a health authority assessor
- Regulatory intelligence and interpreting regulatory guidance
Focus Area
Viral Vector Services
Credentials
Sallie Rosen Kaplan Post-Doctoral Fellow, National Cancer Institute, National Institutes of Health
Doctor of Philosophy in Microbiology and Molecular Genetics from Harvard University
Bachelor’s degree in Biochemistry and Molecular Biology from Michigan State University